셀리버리(대표 조대웅)가 약리물질 생체 내 전송기술 TSDT를 이용한 먹는 고도비만 및 제2형당뇨병 치료신약 CP-SP (Cell-Permeable SOCS3 69-96 Peptide)에 대해 공격적인 임상개발에 본격 돌입한다고 17일 밝혔다.
회사는 이를 위해 CP-SP 펩타이드 신약의 혈뇌장벽 (BBB) 투과능 및 비만 치료효능에 대한 신규 미국특허를 출원 완료했고, 이 펩타이드를 포함하는 구조의 재조합단백질 CP-deltaSOCS3에 대한 유럽연합 (EU) 특허등록 (9월 17일 거래소 공시)에 성공함으로써, 완벽한 지적재산권 (IP) 확보와 동시에 임상개발이 본격화 되고 있다고 설명했다.
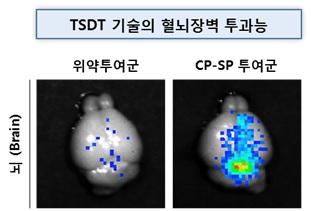
조대웅 셀리버리 대표는 “당사 TSDT 플랫폼기술이 적용된 CP-SP 펩타이드 신약이 혈뇌장벽 (BBB)을 투과하여 뇌조직 깊숙히 위치하며, 전체 뇌질량의 1/100에 불과한 시상하부 조직에 정확히 전달되어 식욕을 억제할 수 있게 한다는 것이 실험적으로 증명되었다. 왜냐하면, CP-SP를 구성하는 aMTD 세포막 투과 펩타이드는 TSDT 플랫폼기술이 제공하는 세포 간 연속 투과성을, 약리물질인 SP 펩타이드는 렙틴-렙틴수용체가 식욕억제신호를 만들어내는 뇌조직, 신경세포에만 타겟팅되는 특성을 조합한 융합펩타이드 표적치료제이기 때문이다” 라고 말했다.
이어 “고도비만 질환동물에 CP-SP를 투여한 후, 뇌조직 내 CP-SP의 전송 분포를 분석한 결과, CP-SP가 뇌 신경세포 및 성상교세포에 전송될 뿐만 아니라, 시상하부 뇌조직에 식욕조절에 관여하는 신경세포 내에도 충분한 양이 전송되었음이 발견되었다. 이것은, TSDT 플랫폼기술의 세포 간 연속전송 메커니즘에 의해 혈뇌장벽을 구성하는 혈관 내피세포 세포막을 투과하고, 계속해서 뇌조직을 구성하는 뇌 신경세포를 연속 투과하여, 렙틴-렙틴수용체가 존재하는 시상하부 뇌세포 내부에까지 전송 가능해야 렙틴저항성을 극복해 식욕억제신호가 우리몸의 식욕을 제어할 수 있게 된다. 셀리버리의 TSDT 플랫폼기술은 이것을 가능케하는 유일한 기술이다” 라고 덧붙였다.
한편 셀리버리는 최근, 미국 뉴저지주의 캡슐 전문제조기업인 캐탈런트와 CP-SP 캡슐 생산계약을 체결함으로써, 먹는 고도비만·제2형당뇨병 치료신약의 본격적인 개발을 알린 바 있다.

