셀리버리(대표 조대웅)가 코로나19 면역치료제 흡입제형 iCP-NI의 영장류 (monkey) 안전성평가시험계약을 글로벌 독성시험기관인 이나리서치 (INA Research, 나가노, 일본)와 체결하여 진행하고 있다고 밝혔다. 중증 및 위중증 환자를 대상으로한 iCP-NI 주사제형 (injectable formulation) 코로나 치료제 개발에 이어, 전체 감염자의 80% 이상인 무증상 확진자 및 경증 코로나19 환자에게 빠르고 편리한 사용이 가능한 흡입제형 (inhalational formulation) 코로나 치료제를 개발중이다.
코로나19 감염병은, 코로나 바이러스 (SARS-CoV-2)에 감염에 의해 종양괴사인자 티엔에프-알파 (TNF-α) 및 인터루킨-6 (IL-6) 등의 강력한 염증성 싸이토카인이 생성되어 면역폭풍 (cytokine-storm) 및 패혈증 (sepsis)에 이르게 되고, 여러 장기가 제 기능을 하지 못함으로써 다발성 장기부전 (multiple organ failure)을 야기하며 심할 경우 사망에 이르게 하는 무서운 질환이다. 코로나19 바이러스 감염병 증상은 급성호흡곤란 증후군 (acute respiratory distress syndrome: ARDS)을 동반하기 때문에, iCP-NI 흡입제형은 구강 및 비강을 포함하는 호흡기관에 직접 분사 흡수되어 코로나 감염병 증세를 치료하는 메커니즘으로 개발하고 있다.
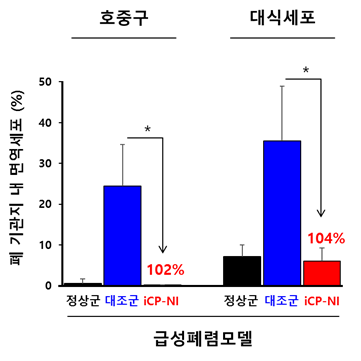
셀리버리 측 iCP-NI 흡입제형 개발책임자는, “코로나 감염병 증상을 모사한 급성폐렴모델에서 진행한 선행연구 결과에 따르면, iCP-NI를 호흡기에 직접 분사한 결과 염증부위의 심각한 조직파괴를 야기하는 면역세포 호중구 (neutrophil) 및 대식세포 (macrophage)가 현저히 감소하였다”고 밝히며, “급성폐렴이 유발되면 면역 T 세포 (Th17)가 과도한 활성을 나타내는데, 이로 인해 증가한 염증성 싸이토카인인 인터루킨 (interleukin)-17의 발현을 iCP-NI가 69% 감소시켜 염증으로 인한 폐 조직 구조의 영구적 손상을 회복시키고, 염증이 발생한 폐 기관지로 백혈구 (leukocyte)를 끌어오는 케모카인 (CCL2 & CCL3)의 생산도 각각 65%와 69% 수준으로 억제하여, 급성폐렴으로 인한 폐 조직손상 치료효능이 발휘되는 것으로 밝혀졌다” 라고 치료효능에 대해 최초로 밝히며 코로나19 치료제로서의 iCP-NI 우수성을 강조했다.
이번 안전성평가시험이 진행되는 이나리서치는 일본 나가노에 위치한 독성시험기관으로 자체 영장류 사육시설을 보유중이며, 50여년 동안 다양한 글로벌 제약사들과 영장류 흡입독성 (inhalation toxicity) 평가시험수행 경험이 있는 베테랑 기관이라 알려져 있다. 안전성평가 비용은 22억 원이며, 성체 필리핀 원숭이 (cynomolgus monkey)를 대상으로 진행되어 iCP-NI 흡입제형 특이적 독성시험결과를 도출하고, 이를 이미 미국 코방스 (Covance, 서머셋, 뉴저지주) 에서 확보된 iCP-NI의 일반 안전성/독성평가 패키지와 취합하여 미국 (FDA)과 유럽 (EMA) 그리고 국내에서 최단기간 내에 코로나19 치료제 임상개발을 하는 것을 목표로 한다고 회사측은 밝혔다.
최근, 국내 메이저 제약사에서 셀리버리에 영입된 독성시험전문 임상개발 책임자는, “이번 iCP-NI 흡입제형의 안전성평가시험의 경우, 이미 미국에서 확보된 iCP-NI 주사제형의 소동물 및 대동물 (영장류) 독성 시험 결과를 그대로 사용하며, iCP-NI 흡입제형 특이적 독성평가만 수행한다. 일반적으로 안전성평가를 위해서는 일반독성시험 (single/repeated dose toxicity), 안전성약리시험 (safety pharmacology), 유전독성시험 (genetic toxicity) 등을 포함하는 풀-패키지 (full-pakage) 시험을 수행하게 되지만, iCP-NI 흡입제형의 독성평가는 대부분의 안전성약리평가 및 유전독성 항목을 생략할 수 있다” 라고 밝히며, “혈관에 투여하는 주사제형과 비교하여, 호흡기에 직접 분사하는 방식의 흡입제형은 호흡기관 조직으로 직접적/국소적으로 약물이 노출되기 때문에 혈중 농도가 상대적으로 낮다. 그러므로, 영장류 1종에 대한 안전성평가 결과만으로 충분히 FDA 기준을 충족할 수 있다” 라고 덧붙였다. 끝으로, “이미 유럽과 미국에서 개발중인 코로나 주사제형 치료제의 안전성평가를 수행하면서, 생체 내 분석법개발을 완료하였기 때문에 iCP-NI 흡입제형은 해당 분석법개발 또한 필요 없으므로 개발속도는 훨씬 더 빠르다” 라고 밝혔다.
셀리버리는, "전세계적으로 독성평가를 위한 영장류 공급이 코로나 감염병으로 인해 원활하지 않은 상황인데도 불구하고 이번 글로벌 독성시험기관인 이나리서치와 신속한 선점 계약을 달성하여, 최단기간 내 코로나19 표준치료제로서 임상개발 완료하겠다” 라고 밝혔다.

